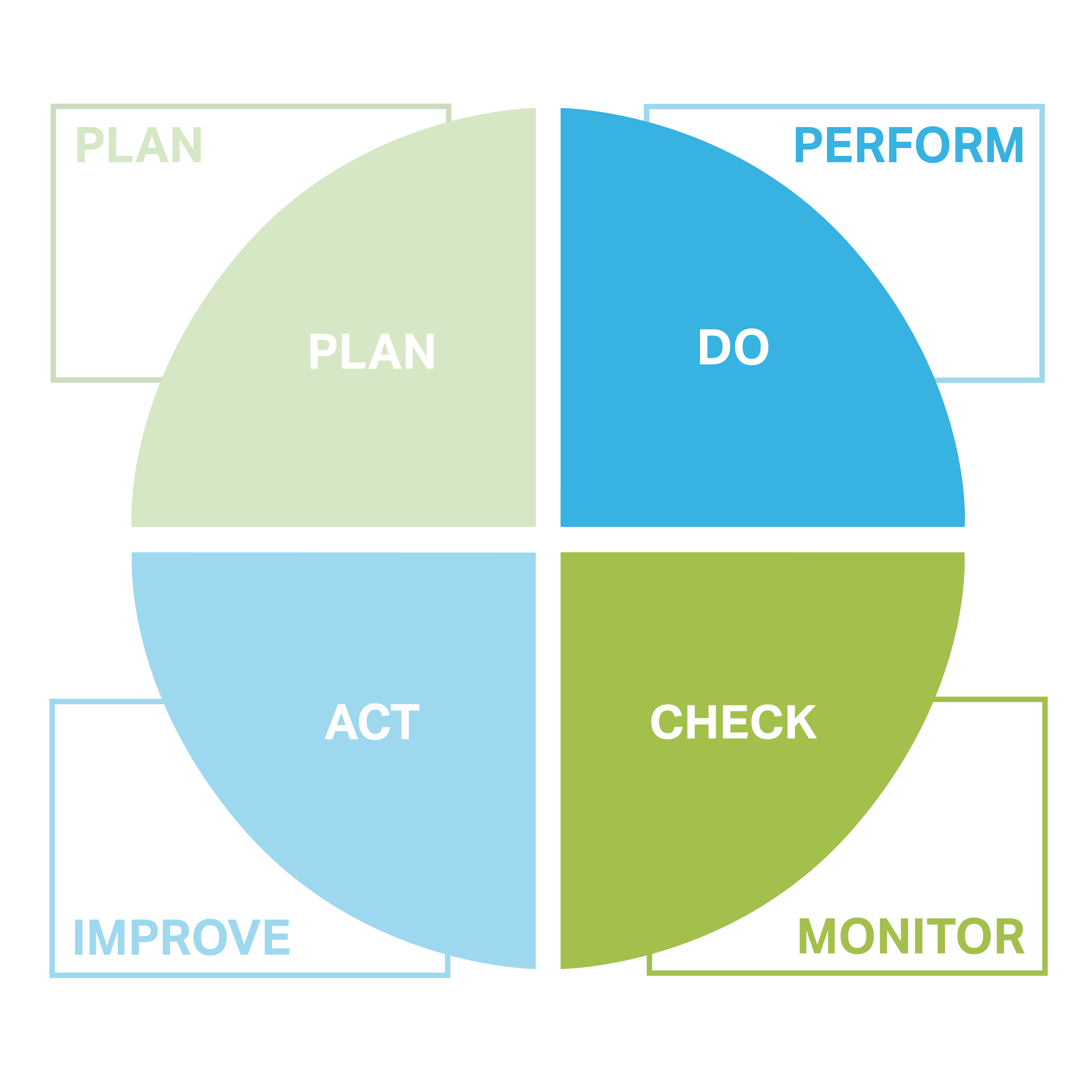
Qualität
Gesetze, Normen und Richtlinien legen ein Framework für Unternehmen regulierter Industrien, wie Pharma und Medizintechnik fest.
Das pharmazeutische- oder medizintechnische Qualitätsmanagement-System (QMS) eines Unternehmens stellt die Summe aller Aktivitäten zur Erlangung und Erhaltung der Compliance dar. Diese unterliegt jedoch Veränderungen der regulatorischen Vorgaben aufgrund von aktuellen wissenschaftlichen Erkenntnissen oder gesundheitspolitischen Entwicklungen. Wir stellen sicher, dass Ihr Qualitätsmanagement-System aktuellen und zukünftigen regulatorischen Anforderungen nationaler wie internationaler Behörden genügt. Die Weiterentwicklung zur permanenten „Inspection Readiness“ sichert und erhält Ihren Zugang zu lukrativen Märkten und stellt einen Mehrwert dar.
Unsere Arbeitsweise zeichnet sich durch eine detaillierte Planung, sorgfältige Durchführung, regelmäßiges Überprüfen, sowie eine gezielte Steuerung von Verbesserungen aus.
Unsere Aufgabengebiete umfassen insbesondere:
WIR
UNTERSTÜTZEN
bei der Optimierung bzw. Einführung eines Qualitätsmanagement-systems
WIR
SICHERN
Ihre Datenintegrität durch Erstellung von Process und Data Flows
WIR
ERSTELLEN
fehlende Dokumente & Trainingsunterlagen zur Einhaltung der Compliance-Anforderungen
WIR
ÜBERNEHMEN
Routineaufgaben im Bereich CAPA-Management, Change Control & Abweichungsmanagement
WIR
BERATEN
zu den Qualitätsmanagement-Risiken bzw. -Grenzen neuer Technologien, wie Cloudservices, BlockChain oder Künstliche Intelligenz
Analyse
Geschäftsprozesse enden nicht an Systemgrenzen, sondern gehen oft darüber hinaus und erfordern daher systemübergreifendes Verständnis. Um Geschäftsprozesse optimal zu unterstützen, arbeiten wir daher an den Schnittstellen zwischen Produktion, Quality, Engineering und IT.
Im Fokus steht der Geschäftsprozess!
Die Identifikation von Lücken hinsichtlich interner und regulatorischer Vorgaben bildet die Basis der Optimierung Ihrer Prozesse und Systeme. Unsere langjährige Erfahrung erstreckt sich auf:
- Warenwirtschaftssysteme (ERP)
- Dokumentenmanagemensysteme (DMS)
- Labor-Informationsmanagemensysteme (LIMS)
- Enterprise Qualitätsmanagementsysteme (eQMS)
- Manufacturing Execution Systeme (MES)
- oder Produktionsanlagen.
In enger Zusammenarbeit erarbeiten wir mit Ihnen die Anwendungsfälle (“use cases”) und leiten daraus Ihre spezifischen Anforderungen ab.
Wir begleiten Sie bei der Implementierung, Überprüfung und Sicherstellung Ihrer Prozesse und Systeme.
Zur Identifikation der Anforderungen und Prozesse bedienen wir uns folgender Methoden:
Experteninterviews
Abteilungsworkshops
Fragebögen
Arbeitsplatzanalysen
Anforderungs- / Geschäftsprozessmanagement in 4 Schritten:
Durch unsere systematische Vorgehensweise analysieren, dokumentieren, bewerten und gliedern wir Ihre Anforderungen und Prozesse.

Identifikation
Wie sieht meine Anforderung bzw. mein Geschäftsprozess aus?

Dokumentation
Beschreibung der Anforderung bzw. des Geschäftsprozesses

Gliederung
Welche Anforderungen bzw. Geschäftsprozesse gehören zusammen?

Bewertung
Welche Anforderungen bzw. Geschäftsprozesse brauche ich wirklich?
Validierung
In regulierten Industrien, wie z.B. Pharma und Medizintechnik legen Gesetze, Normen und Richtlinien fest, dass IT-Infrastruktur, wie Server oder automatisierte Produktionsanlagen, qualifiziert und computergestützte Systeme, die sich dieser Infrastruktur bedienen, sowie Prozesse validiert werden müssen.
Hersteller sind verpflichtet im Rahmen solcher Qualifizierungen / Validierungen den dokumentierten Nachweis zu erbringen, dass ein System oder ein Prozess die vorher spezifizierten Anforderungen (in Form von Akzeptanzkriterien) im praktischen Einsatz dauerhaft und reproduzierbar erfüllt.
Ein einmal erreichter qualifizierter / validierter Zustand muss dauerhaft aufrechterhalten werden.
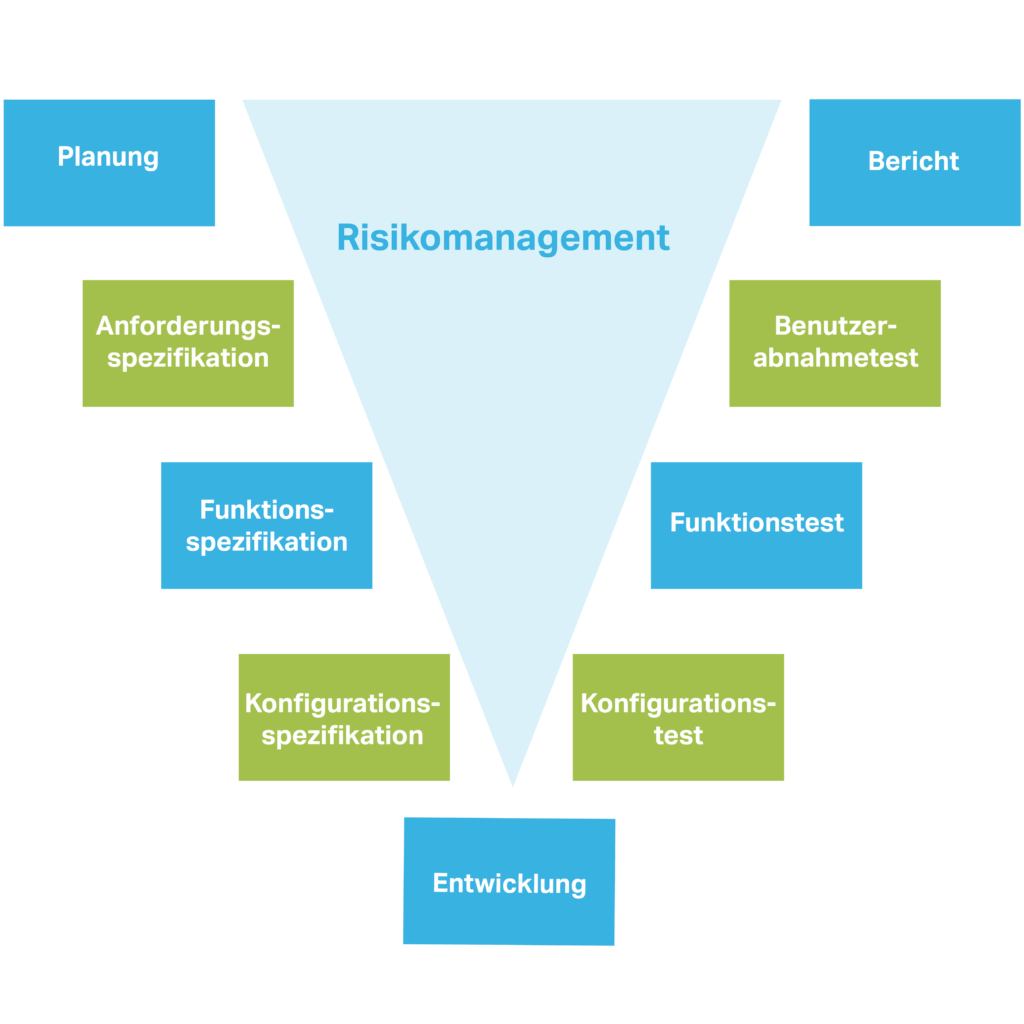
Wir unterstützen Sie bei der Planung, Durchführung, Überprüfung und Verbesserung Ihrer Qualifizierungs- und Validierungsprojekte und orientieren uns dabei an Ihrem Change Management Prozess, der zentraler Bestandteil Ihres pharmazeutischen / medizintechnischen Qualitätssystems ist.
Planung:
- Analyse von Anforderungen und Geschäftsprozessen
- Validierungsplan
Spezifikation:
- Anforderungsspezifikation
- Funktionsspezifikation
- Konfigurationsspezifikation
Verifizierung:
- Benutzer-Abnahme-Test, Funktions- und Konfigurationstest
- Testmanagement (Koordination der Testerstellung und ‑durchführung)
- Defektmanagement (ggfs. Überführung zur Nachverfolgung in CAPAs)
Bericht:
- Testbericht
- Validierungsbericht
MES
Ein Manufacturing Execution System (MES) ist ein umfassendes, dynamisches Softwaresystem, das den Herstellungsprozess vom Rohmaterial bis zum fertigen Produkt steuert, überwacht und dokumentiert.
Es bildet die Schnittstelle, zwischen einem Warenwirtschaftssystem (ERP) und einem Prozessleitsystemen und liefert Daten, die benötigt werden, um die Produktion effizienter zu gestalten, Mitarbeiter durch den Prozess zu führen und den Herstellungsprozess vollumfänglich zu dokumentieren.
Manufacturing Execution Systeme werden in der Life Science-Branche hauptsächliche genutzt, um Herstellungsrezepte (Master-Batch-Records) zu erstellen und diese gepaart mit konkreten Auftragsinformation abzuarbeiten. Ein bedeutender Nutzen eines MES besteht darin, den Herstellprozess in Echtzeit zu überwachen, so dass noch ggfs. frühzeitig eingegriffen werden kann.
Außerdem bieten ein MES die Option die Herstellungsdaten durch Review by Exception freizugeben, was den Prüfungsaufwand deutlich reduziert.
Durch die Nutzung eines MES könne Sie Ihre Kapazitäten und Ressourcen optimal einsetzen, die Durchlaufzeit und den Umlaufbestand reduzieren und den Arbeitsaufwand für die Planungsaufgaben minimiert. Bei Verwendung in der Life Science Branche ist sicherzustellen, dass das Manufacturing Execution System gesetzes- und richtlinienkonform betrieben wird, GxP Anforderungen erfüllt werden und der dokumentierte Nachweis erbracht wurde. Zusätzlich muss die Datenintegrität sichergestellt werden.
Hierfür können z.B. folgende Leitlinien / Normen hilfreich sein:
- ISA88
- ISA95
- GAMP5
Wenn Sie eine neutrale, herstellerunabhängige Beratung wünschen und
Unterstützung bei der Umsetzung (Planung, Projektierung, Projektleitung, / Projekt-SMEs, MBR Designer) oder der Weiterentwicklung eines MES-Systems benötigen, stehen unsere fachkundige Mitarbeiter Ihnen gerne zur Seite.

Projekte
Sie haben das Projekt – Wir haben die Ressourcen!
Gerne unterstützen wir Sie bei Ihrem Projektmanagement (nach Prince2 / PMI). Wir übernehmen für Sie die zielorientierte Initiierung, Planung, Durchführung, Überwachung, Steuerung und Führung Ihrer Projekte.
Unsere Projektmanager begleiten Sie in den folgenden Schwerpunkten:
Analyse des Umfelds (Stakeholder)
Planung von Projektphasen inkl. Meilensteine
Erstellung des Projektstrukturplans mit Arbeitspaketen
Festlegung der Projektrollen (Verantwortlichkeiten, Kompetenzen)
Durchführung des Projekts und Unterstützung bei Zeit- / Terminmanagement, Kosten- und Ressourcenmanagement, Kommunikationsmanagement und Risikomanagement
Erstellen der Dokumentation (Transparenz und Nachvollziehbarkeit der Ergebnisse)
Formulierung der “Lessons Learned”

Datenintegrität
Daten, die beim Herstellungs- und Qualitätsmanagementprozess von Arzneimitteln erfasst wurden stellen eine wesentliche Informationsquelle dar, um Aussagen bezüglich der Sicherheit, Qualität, Identität, Reinheit und Wirksamkeit dieser Arzneimittel treffen zu können.
Datenintegrität betrachtet die Genauigkeit, Vollständigkeit, Vertrauenswürdigkeit und Konsistenz von Daten über den gesamten Lebenszyklus, was oft durch die Akronyme ALCOA (Attributable, Legible, Contemporaneous, Original, Accurate) bzw. ALCOA+ (zusätzlich Complete, Consistent, Enduring, Available) dargestellt wird.
Gesetzliche Anforderungen stellen hierfür u.a. der 21 CFR Part 11, 210 und 211der FDA als auch der EudraLex der EMA dar.
Die Integrität von Daten steht seit Jahren im Fokus von Inspektionen und Audits. Zusätzlich zur Sicherung der Produktqualität wird von der Industrie / den Behörden eine klare Strategie gefordert, wie die Integrität kritischer Daten über deren gesamten Lebenszyklus gesichert werden kann.
Wir helfen Ihnen Fehler in diesem Bereich zu vermeiden, die Dokumentation von Anfang an systematisch zu organisieren und ihre Daten über den gesamten Lebenszyklus unter Kontrolle zu halten.
Unsere langjährige Erfahrung erstreckt sich auf:
- Erstellen von Datenflussdiagrammen
- Durchführen von GAP – Analysen
- Risikobewertungen
- Festlegen von risikobasierten Maßnahmen und deren Nachverfolgung
Wenn Sie wollen übernehmen für Sie die Initiierung und Planung ihrer Datenintegritätsstrategie und begleiten sie bei der Durchführung.







